12月4日。 あってはならない 「睡眠剤混入」 小林化工 のジェネリック薬の驚愕のニュースが、Web上で駆け巡った。
・・・
福井県は 4日、同県あわら市の製薬会社 小林化工 が、爪水虫など皮膚病の治療に使う経口抗真菌剤イトラコナゾール錠50「MEEK」約10万錠分を自主回収すると発表した。
製造過程で通常の服用量を超える睡眠導入剤成分が混入し、岐阜、大阪、佐賀の3府県で計12人に意識消失や強い倦怠(けんたい)感などの副作用が確認されたという。
小林化工 によると、イトラコナゾール錠は、白癬(はくせん)菌が原因で爪が白く濁り爪水虫とも呼ばれる「爪白癬」などの治療に使う医療用医薬品。
12月1~3日に 2~77歳の 男女 12人 に副作用が確認された。
約半数は回復に向かっているが、岐阜県の男性(59)が救急搬送され、入院した。
同錠剤を服用して首都圏の病院に入院していた患者の 70代女性が死亡した。
同社は、あわら市の本社工場で原料を量る担当の社員が、入れるべき成分と睡眠導入剤の成分「リルマザホン塩酸塩水和物」を 取り違え、保管場所から持ち出したのが原因と説明。
本来は 2人一組で確認が必要だったが、1人で作業 していた。
同社の 小林広幸社長は 4日、記者会見し
「誤混入の原因はヒューマンエラーであり、医薬品企業として万が一でもあってはならない。患者や医療機関の皆さまに深くおわび申し上げる」と陳謝した。
回収対象はロット番号「T0EG08」と刻印され、9月28日以降に出荷された商品。
全国の医療機関などに流通しているとみられる。〔共同〕
(日本経済新聞 WEB NEWS の発表記事)
・・・
上記についての 連絡先 電話番号は 0120-37-0690
翌日 5日。 今度は 回収対象の提供画像の誤りを発表。
・・・
医薬品製造販売の 小林化工 (本社福井県あわら市)は 12月5日、自主回収している同社製造の経口抗真菌剤「イトラコナゾール錠50『MEEK』」について、4日に報道各社に提供した写真は回収対象ではない別の錠剤だったと訂正した。
回収対象の錠剤シート表面には「Meiji」と記されており、裏面は銀色となっている。
正しい画像
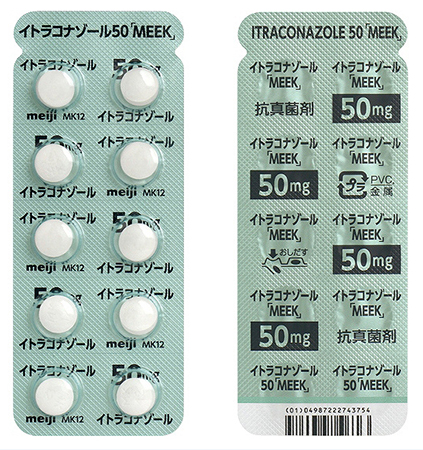
誤提供画像

イトラコナゾール錠は 爪水虫やカンジダ症などの治療薬。
回収対象の錠剤は販売元の「Meiji Seika ファルマ」 が、9月28日以降に出荷した 100錠入り929箱。
錠剤シートに製品ロット番号「T0EG08」と刻印されている。
福井新聞 WEB NEWS より一部抜粋
・・・
7日 「イトラコナゾール錠『MEEK』」全3種の製造を中止し、全てのロットを自主回収すると 同社ホームページで発表した。
新たな回収対象は、同社と製薬会社「Meiji Seika ファルマ」が販売している
イトラコナゾール錠50 / 同100 / 同200
使用期限は 2020年12月~23年10月の製品
12月12日 には、このジェネリック薬服用により、関東地方在住の 70歳代女性が死亡。
なぜ、あってはならない 「睡眠剤混入」 が起きたのか?
小林化工 によると、製造工程で原料を計量する際に、社員が睡眠導入剤の成分の リルマザホン塩酸塩水和物 を、誤って混入したと発表。
同社の規定では1人が作業し、もう1人が立ち会ってダブルチェックするが、当時は1人で作業していたという。
混入した リルマザホン塩酸塩水和物 は、睡眠導入剤で通常使用する最大投与量の 2.5倍 に 及び、岐阜県では 副作用のため車の運転を誤り、事故を起こしたケースもあったという。
小林化工 イトラコナゾール錠50「MEEK」[ロット番号:T0EG08] 服用による健康被害の状況 をウェブサイトに掲載中。
最新の 健康被害状況 を更新(1月3日時点)
これまでに認められた主な症状
眠気 頭部ふらつき感 傾眠 意識障害 転倒 意識消失 めまい感 記憶障害 ろれつ不良 倦怠感 意識レベルの低下 など
自主回収による混乱
小林化工 が自主回収を進めている「イトラコナゾール錠 50『MEEK』」は、該当薬を交付した病院内処方または、院外処方の薬局にて、患者が持参した回収品を代替薬に交換するが、医療機関の再受診や処方箋の必要性に関する明確な見解がないことから、一部の薬局で、交換時の対応と費用負担等について混乱が生じている。
12月4日 から 自主回収(クラスⅠ)を開始
イトラコナゾール錠 50『MEEK』に、ベンゾジアゼピン系睡眠薬・リルマザホン塩酸塩水和物が 1錠 当たり 5mg 混入 していた。
混入したリルマザホン塩酸塩水和物の 通常用量は 2mg で、通常療養の 2.5倍 に当たる。
イトラコナゾールの通常用量は 400mg(50mg であれば 8錠)であることから、通常に摂取した場合、1日の接取量は通常用量の数十倍にのぼった可能性がある。
ただ、同剤の推定致死量は 0.05 ~ 0.5g/kg とされており、致死量には至らないという。
この原因を特定する過程で、イトラコナゾールの製造過程で用量を下回ることを防ぐために追加で同剤を加えていたことや、手順書に2人で行うことが義務付けられていた作業を1人で実施するなど、承認書にない製造行程を実施していたことも判明した。
12月7日 から、クラスⅠ 以外の全ロットを自主回収(クラスⅡ)
12月16日。 従業員が製造過程で睡眠導入剤成分を投入したことを示す作業記録が残っていたことが 福井県への取材で分かった。
新たに会社の品質管理やチェック機能が不適切だった疑いが出てきた。
投入されるはずのない成分が記録されていたことなどから、作業を熟知していない従業員が誤って投入し、その後の工程でも会社がチェックしていなかった疑いが出てきた。
県などは安全確認を怠ったとして、業務停止命令を視野に行政処分を検討している。
睡眠導入剤の成分が混入していたのは 経口抗真菌剤のイトラコナゾール錠50「MEEK」。
2020年6,7月に製造し、9~12月に出荷したもの。
小林化工 によると、薬の製造過程で原薬の量が減ることがあり、成分を追加する作業を行う際に睡眠導入剤「リルマザホン塩酸塩水和物」を誤って投入したという。
作業記録に、この睡眠導入剤を示す番号が記載されていた。
小林化工の説明では、混入が起きたのは、加工途中に目減りした原料をつぎ足す作業で発生したという。
同錠剤の工程は、原料の計量や乾燥、粒子の均一化など数日にわたる。
そのため、有効成分であるイトラコナゾールは機械に付着するなどして目減りする。
この作業はチェック役と2人一組で行う規程であるが、当時は1人で行っていたという。
しかし、足りないからと補充した爪水虫治療薬の成分と睡眠導入剤の成分は全く異なり、
しかも、それぞれ見た目の違う容器に入っていたという。
本来投入する爪水虫治療薬の成分 イトラコナゾール は 高さ1メートルほどの大きな紙製の容器 に、睡眠導入剤の成分 リルマザホン塩酸塩水和物 は 高さ15センチほどの菓子箱のような小さな平の缶 に保管されていた。
小林化工 は「ラベルもロット番号も違う。一般的に取り違えるレベルではない」とする。
工場にはバーコード管理などはなく、人の手で確認していた。
6~7月の製造で、担当者の記憶もはっきりしないという。
成分の追加投入は今回の場合、医薬品の成分が均等に拡散されずに錠剤の濃度にばらつきが出る可能性があることから、厚労省が承認した製造手順では認められていない。
また出荷前の 7月、薬の含有成分を調べるために「液体クロマトグラフィー」と呼ばれる手法でサンプル調査した際、異物の混入を示唆するデータが検出されたが、見過ごされた疑いも明らかになっている。
分析結果は成分ごとに含有量が「波」の大きさで示される。
出荷前の調査では、通常では検出されるはずのない成分の混入を示す「波」が確認できた。
異物混入の疑いを示唆するものだが、波が小さいことなどから気付かなかったという。
そこで、9~12月に出荷した。
健康被害が12月に報告され、このデータを再検証したところ睡眠導入剤の混入の可能性が浮上。
この作業記録を確認して睡眠導入剤の誤投入が分かった。
小林化工 は「出荷前に詳しくデータ分析していれば混入に気付けたかもしれない」と話した。
医薬品医療機器法は、製薬会社が製造手順を作成して記録し、それらを基に品質をチェックして医薬品を出荷するよう義務付けている。
同社の内規では、成分の取り出しや計量は2人1組で指さし確認をしながら進めると定められているが、今回は担当者が1人で作業していた。
睡眠導入剤の投入が記された作業記録やサンプル調査の分析結果も含め、あらゆる過程で安全性がチェックされていなかった疑いがある。
厚労省の担当者は「記録をしっかり確認するなどしていれば、そのまま出荷するようなことは考えられない」と話した。
その後の状況について
12月17日 には、問題となった薬を処方された患者に対し、一律 30万円の慰謝料や、必要となった治療費などを補償すると発表
また、弁護士や医薬品分野の専門家で構成する第三者委員会を設置し、事実関係の解明などを行うと発表した。
12月21,22日。 医薬品医療機器法に基づいて、厚生労働省と福井県、それに医薬品を承認審査する医薬品医療機器総合機構(PMDA)が、経口抗真菌剤イトラコナゾール錠50「MEEK」(ロット番号・製造番号:T0EG08)の製造工程で睡眠剤が混入され、死亡例を含む健康被害を生じたことから、 小林化工 を立ち入り調査した。
12月25日。 当該製品を販売する科研製薬は、小林化工が製造販売元で同社が販売する「ブシラント錠100」(対象ロット・T8DE05)についても、「再確認の必要性が確認された」として、自主回収(クラスⅡ)すると発表
回収対象製品「ブシラント錠100」(T8DE05)
包装規格PTP100錠(出荷時期:2018年6月8日~2018年7月2日)
包装規格PTP500錠(同:2018年6月8日~2018年6月14日)
いずれも使用期限は 2021年4月
科研製薬によると、「保存していた製品の再試験の結果、問題点は確認されてはおらず、重篤な健康被害が発生するおそれは無い」としながらも、「更に安全性に万全を期すため、自主回収する」と説明している。
医療関係者に対する自主回収(クラスⅡ)の情報提供は25日から開始している。
同社としては2021年2月26日までに当該製品について回収する方針。
あってはならない 「睡眠剤混入」 が発覚したきっかけ
11月27日に、岐阜県高山市の久保賢介医師(63)に、救急病院からの連絡があったことが発覚のきっかけであった。
59歳の男性が車を運転中に意識を失い、溝に脱輪したという。
久保医師は、内科とアトピーの治療を専門とする有床診療所の院長で、
59歳男性の救急搬送以後、入院患者4人についても普段と様子が違っていることに気が付いた。
朝食を食べたら夜まで寝ていたり、起こすと記憶を一部失っていたりすることがあった。
他の外来患者も、12月2日の朝には30代女性が意識がもうろうとした状態になり寝てしまった。
32歳の男性は配送の仕事中にトンネル内で意識がなくなり、センターラインのポールに衝突した。
本人は当時の記憶がなく、事故後も、もうろうとしたまま仕事を続けたという。
意識障害があった患者7人には共通点があった。
久保医師は「全てイトラコナゾールが原因だと確信した」
販売元の「Meiji Seika ファルマ」に報告。
上記の状態の他、4日間にわたってほとんど目を覚まさなかった入院患者もいた。
全員がロット番号「T8DE05」の薬を服用していた。
小林化工によると、同錠剤による副作用の報告は、12月に入ってから1日に2人、2日に1人だった。
しかし「医薬品の副作用の症例報告は毎日入っており、まだ(健康被害という)認識はなかった」と幹部は振り返る。
3日になって岐阜の久保医師から7人、他府県から2人の計9人の副作用の報告があり、事の重大さにようやく気が付いた。
4日、服用した2歳女児を含む患者12人に健康被害があったと発表した。
今回、重篤例を含む多数の健康被害が報告されているイトラコナゾール錠50「MEEK」(ロット番号:T0EG08)の販売元である 医薬品製造業 Meiji Seikaファルマ は 12月11日付で、小林化工が製造する販売製品全品目を出荷停止すると特約店に伝達した。
対象品目はレボフロキサシン錠やピタバスタチンCa錠など43品目85包装。
同社はすでに小林化工の現地調査を開始しており、結果が判明するまでは小林化工の製造品の出荷を停止する方針。
供給再開の時期については、改めて案内するとしている。
出荷停止はオザグレル、クラリスロマイシン、ピタバスタチン、バラシクロビルなど
出荷停止の対象製品には、小林化工が製造販売元となる オザグレル や クラリスロマイシン、 リスペリドン などのほか、Meiji Seikaファルマ が製造販売元である ピタバスタチン や バラシクロビル などが含まれる。
小林化工 の企業体質に問題はないか?
小林化工 は 1961年設立。
安価な後発医薬品(ジェネリック医薬品)の 製造や販売を行っている。
扱う商品は、アレルギー性疾患の治療薬や抗生物質製剤が中心。
会社の規模は今年3月期の売上高が370億円。従業員数 800人。
先発医薬品を生産する大手の製薬会社と異なり小さな組織である。
問題の薬「イトラコナゾール錠50『MEEK』」は 市販薬ではなく、医師の処方箋がなければ購入できない薬だ。
肝臓への負担が大きく、肝機能検査等を行い、医師の処方で服用可能になる。
目減りした原料を追加する作業で、担当者が成分の入った容器を取り違えたという、一見、単純なミスのように思われるが、追加の作業は厚労省の承認を得ていない。
容器の違いも明らかで、正常な人間が間違える類のミスでもない。
さらに、2人一組で確認するという社内規定に従わず、品質検査で異物の混入が疑われたにもかかわらず、そのまま出荷していた。
業界関係者によると、加工途中で有効成分の量が減ることはあるが、あらかじめ多めに投入すれば済むことで、コスト抑制のため有効成分をぎりぎりの量にして後でつぎ足していたのかもしれないという。
これは、本来はやらない行為であり、工程が増えれば、その分エラーは起きやすくなると話す。
実際、原料をつぎ足す行為自体が厚生労働省が承認した手順にないことも判明している。
小林化工の幹部は「管理側と現場とで認識の違いがある」と釈明し、第三者機関を通じた調査で明らかにしたいとした。
当初の健康被害の報告にも、医薬品は毎日、副作用の報告が上がるため、問題視していなかったと言う。
厚労省が承認した製造の手順やダブルチェック、品質検査をことごとく無視し、報告をクレームと切り捨て、自らの会社に起こっている問題意識として感じていない。
こうして、工程・品質管理を問われるミスがいくつも重なり、問題のロットは全国に出回った。
大手製薬会社幹部は「自社で睡眠導入剤も製造しているが、原料の管理は厳重だ。なぜいとも簡単に間違えたのか信じられない」
「小林化工が作っている製品を全て調べて、白黒付けないと安心して扱えないだろう」
日本ジェネリック製薬協会は「協会全体に関わる重大な問題と受け止めている」とのコメントを発表し、会員企業約40社に管理を徹底するよう通知を出した
薬には、開発費と時間がかかる。
先発薬ではなく、後発薬(ジェネリック)は、言いかえると、安い費用で手間を掛けずに製造できるため、費用を抑えて利益追求に邁進できる。
ネット上の意見の中に、「小林化工は毎年のように自主回収を繰り返している。今回のように、自主回収せずに、内密に処理したケースはなかったのか。」という疑問の声が上がっている。
ジェネリック医薬品が一般に普及してきた昨今、一般市民に、こうした不安を抱かせる小林化工の罪は重い。
「小林化工による薬の自主回収は、この4年間で5件目だ。昨年10月には、胃潰瘍などの治療薬に発がん性物質が含まれていたことが判明した。今回と同様、厚労省の定めた3段階の危険度で、最も重大なケースに該当している」という声もある。
昨年の2019年10月に自主回収された 胃潰瘍治療薬 ラニチジン錠150「KN」 は、胃・十二指腸潰瘍などの治療薬「ラニチジン塩酸塩錠」の原薬が中国で製造されており、許容限度値を超えた発がん性物質が検出されたとの情報を受け回収した。
これに関しては 小林化工だ けでは無く、先発メーカーを含め、ほぼすべてのメーカーが回収を行っている。
ラニチジンの回収は健康被害は出ていない状況での予防的措置として回収している。
ラニチジンの構造上、発がん性物質の発生リスクをを完全になくすことは難しい製剤である。
こうした知識を、薬を飲む側も知って、自分で選択できる賢さをもたねばならないのかもしれない。
いつもの薬なのに、自分の体がいつもと違うという、自分の内の声に気づくことが、健康を守るために、大切なことなのかもしれない。
薬の原料や製造・加工の過程、そして、処方まで、すべてをクリアにすること、消費者も、ただ与えられるものをそのままに受け入れるのではなく、自ら学び知ることが重要だ。
ジェネリック医薬品とは
ジェネリック医薬品は、厚労省の認可を得て製造され、新薬と同等の効き目が保証され、研究開発費を伴わないため比較的安価で流通できる。
これまでの『安かろう悪かろう』の風評を受けてきたが、信頼を得るため業界全体で啓蒙に取り組んできた結果、今年 9月時点で 政府目標の 80%に近い 78.3%まで使用割合を拡大させた。
だが地道に得てきた信用も、一つの事故で失墜する。
厚労省と業界団体が、どこまで各社の管理体制を確認できるのか、教育についても再考が必要だ。
社会保障における、医療費の高止まりを是正するうえでも、ジェネリック薬の存在は重要である。
製薬会社は、国民の生命と国民の働いたお金で支払われた税金を大切に使うという
高貴な働きのひとつであることを、末端の社員一人一人に啓蒙していくことが、薬害を予防することになるのではないだろうか。
当協会では、毎月4日に、認知機能改善にお役立ていただけるメールマガジンを配信しております。
TOPページ にございます 無料メールマガジン登録フォームよりご登録をお願い申し上げます。
(Photo by Miko Guziuk on Unsplash)

